Профессор Университета Иннополис вместе с международной командой учёных, возглавляемой профессором университета Стони Брук Дмитрием Козаковым, разработали сверхбыстрый метод моделирования белковых взаимодействий, открывающий новые возможности для исследователей в биохимии, биомедицине и ускоряющий разработку вакцин и лекарств.

Многие современные лекарства имеют побочные эффекты – помимо лечения больного органа, они воздействуют на органы и клетки, которые не нуждаются в этом. При раковых заболеваниях химиотерапия воздействует на опухоль и сказывается на здоровых органах. Перед учеными стоит сложная задача: как быстрее доставить лекарство к больным клеткам организма, не затрагивая здоровые, где оно начнет взаимодействие с нужными белками.
Белок — основной строительный материал клетки. В типичной клетке живого организма одновременно происходят сотни тысяч белковых взаимодействий. Изучение характеристик этих взаимодействий поможет учёным приблизиться к важным открытиям: лучше понять, как функционируют живые организмы, разработать новые методы лечения опасных заболеваний, разобраться, как лекарство укладывается в клетку и облегчить создание новых биоматериалов для изобретения медикаментов. Белковые взаимодействия изучают в лабораториях в модельных экспериментах (in vitro) или с помощью компьютерное моделирование.
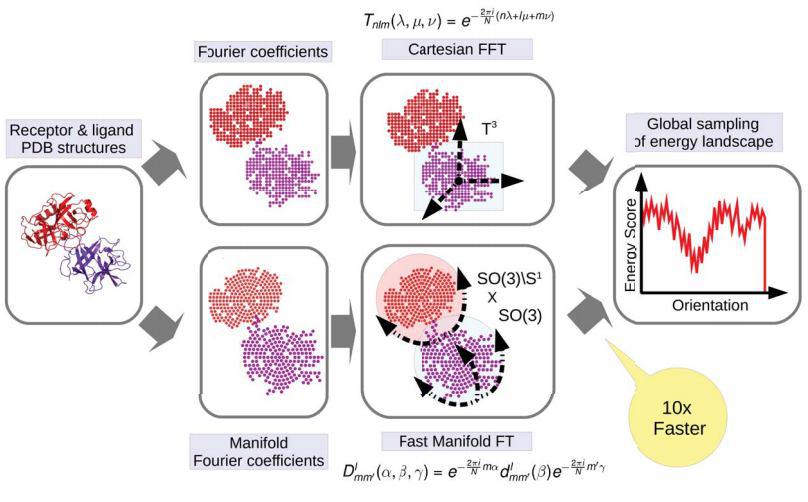
Ярославу Холодову, профессору Университета Иннополис, в течение нескольких лет совместной работы с международной командой ученых из России, Франции и США, возглавляемой профессором Дмитрием Козаковым, куда также входили Андрей Казеннов и Дмитрий Подгорный, удалось разработать и реализовать алгоритм компьютерного моделирования, который способен в десятки раз быстрее аналогичных систем предсказывать структуры белковых комплексов, образующихся при связи двух белков друг с другом. Данное открытие поможет понять, что биологические процессы представляют собой на молекулярном уровне и как на них повлиять.
 «Лабораторные эксперименты дорогие, так как требуют использования сложного оборудования и реагентов — объясняет профессор Холодов, — их используют крупные исследовательские лаборатории, небольшим научным группам доступнее использовать компьютерное моделирование».
«Лабораторные эксперименты дорогие, так как требуют использования сложного оборудования и реагентов — объясняет профессор Холодов, — их используют крупные исследовательские лаборатории, небольшим научным группам доступнее использовать компьютерное моделирование».
В мире разработано десяти компьютерных систем прогнозирования для расчета белок-белкового взаимодействия, однако они плохо приспособлены для того, чтобы моделировать большое количество белковых взаимодействий одновременно: каждый подобный комплекс требует при моделировании много часов работы суперкомпьютера и финансовых затрат на энергопитание. Эти проблемы и побудили команду учёных разработать новый сверхбыстрый метод моделирования белковых взаимодействий.
«Формирование белкового комплекса происходит с использованием трехмерных структур двух белков, которые позволяют спрогнозировать с большой точностью его структуру. Задача совсем не проста, в том числе и с точки зрения вычислений, ведь для нахождения правильной ориентации двух белков необходимо проанализировать миллиарды различных конфигураций», — комментирует Ярослав Холодов, подчеркнув, что статья с описанием метода опубликована в журнале PNAS.
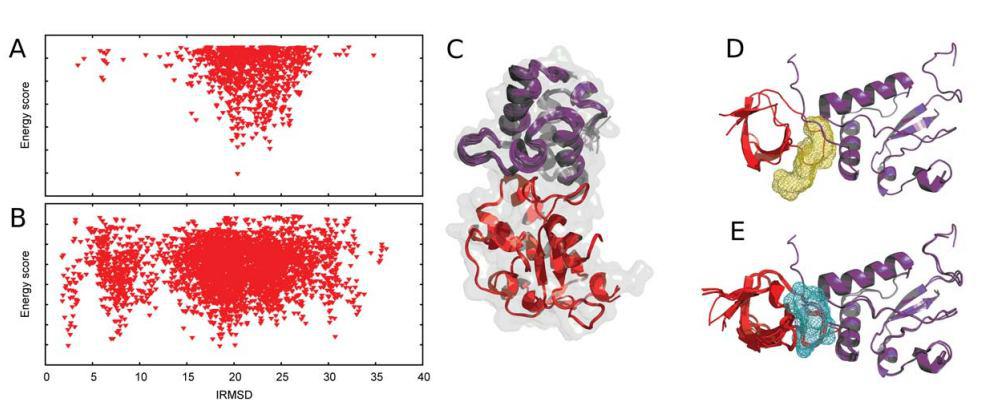
Чтобы понять сложность и объем работы, профессор предлагает сравнить этот процесс с конструктором Лего: представить, сколько всевозможных конфигураций можно создать из 1000 кубиков — по такому же принципу создается множество белковых соединений.
И если существующие алгоритмы проводят мониторинг каждой отдельной конфигурации независимо друг от друга, то новая разработка ученых позволяет практически мгновенно провести анализ одновременно всех комплексов, что ускорят процесс в 10-100 раз. К тому же, как утверждает Ярослав Холодов, скорость не ухудшает точности вычислений. К плюсам разработки относится и тот факт, что алгоритм в вычислительном отношении менее затратный при использовании дополнительных взаимосвязанных функций по сравнению с классическими подходами.
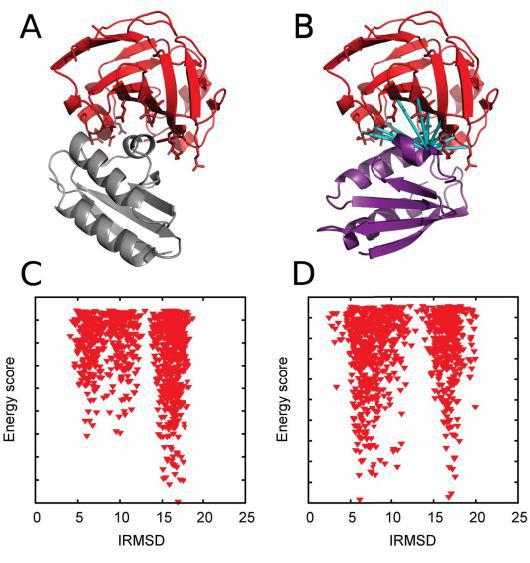
Воспользоваться алгоритмом может любой желающий — он стал новой вычислительной начинкой публичного сервера ClusPro, созданного той же командой ученых. ClusPro — специализированный компьютерный сервер для расчета белковых взаимодействий, представляющий онлайн-сервис. Этот сервис используют на сегодняшний день в своей работе около 10 000 исследовательских групп.
На мировом чемпионате компьютерных систем прогнозирования белковых комплексов, проведенном CAPRI (критическая оценка предсказанных взаимодействий) в Тель-Авиве в этом году, ClusPro признали лучшим автоматическим сервером — он чаще других угадал правильную структуру белок-белкового комплекса.
Как отмечает Ярослав Холодов, данная разработка — удобный инструментарий для людей, занимающихся фундаментальной наукой, которые, благодаря открытому доступу к сервису, могут вывести свои исследования на новый уровень.


